Экспериментальная психология
2012. Том 5. № 2. С. 119–134
ISSN: 2072-7593 / 2311-7036 (online)
Магнитоэнцефалография – новейший метод функционального картирования мозга человека
Аннотация
Общая информация
Ключевые слова: магнитоэнцефалография (МЭГ), картирование мозга, современные методы нейровизуализации, нейроимиджинг, речь, предоперационная диагностика, эпилепсия
Рубрика издания: Методы исследований
Тип материала: научная статья
Для цитаты: Шестакова А.Н., Буторина А.В., Осадчий А.Е., Штыров Ю.Ю. Магнитоэнцефалография – новейший метод функционального картирования мозга человека // Экспериментальная психология. 2012. Том 5. № 2. С. 119–134.
Полный текст
Введение
В последние десятилетия кардинальным образом изменился характер экспериментальных исследований в области нейронаук в целом и изучения деятельности мозга человека в частности. Основополагающими принципами развития фундаментальных и прикладных исследований мозга стали междисциплинарный подход и деятельность на стыке естественных, точных и гуманитарных областей знания. Вместе с тем, благодаря развитию физики низких температур, нелинейной оптики, электроники, вычислительной техники, математического моделирования, статистики и нанотехнологий в мире произошел прорыв в области визуализации мозговых процессов во времени и пространстве. Группа появившихся новых методов, позволяющих проводить неинвазивные исследования мозга, получила общее название «нейроимиджинг» (от англ. neuroimaging; дословно – визуализация, отображение нервных процессов).
Магнитоэнцефалография (МЭГ) – одна из уникальных инновационных технологий нейроимиджинга. Данный метод позволяет с высокой точностью локализовать источники нейронной активности в пространстве и времени. Наряду с фундаментальными исследованиями, такими, как исследования сенсорных и моторных функций мозга и когнитивных процессов памяти, внимания, речи и т. д., МЭГ дает возможность неинвазивной локализации эпилептических очагов патологической нейронной активности и дифференциальной диагностики различных форм эпилепсии, что позволяет осуществлять предоперационную диагностику.
1. Общие принципы обработки данных магнитоэнцефалографии
1.1. Магнитоэнцефалографическое картирование источников нейронной активности
Мозговые процессы, реализующие механизмы восприятия и более высокоуровневые когнитивные функции, протекают с высокой скоростью. Так, от наружного уха до первичной слуховой коры звуковой сигнал доходит за 20 мс, после чего, – например, в случае предъявления слов на слух, – сигнал распространяется в зоны, связанные с речью и языком, максимум за 100–200 мс (Eldredge, Miller, 1971; Shtyrov et al., 2010 b), проходя на каждом этапе сложную обработку во всех задействованных областях мозга. Очевидно, что для понимания таких механизмов необходимо иметь возможность локализовать их не только в пространстве, но и во времени. Появившиеся в последние десятилетия современные методы отображения гемодинамических процессов, например, функциональная магнитнорезонансная томография (фМРТ) или позитронно-эмиссионная томография (ПЭТ), позволяют получить точную (до нескольких миллиметров) пространственную локализацию. Однако их временное разрешение (несколько секунд) на несколько порядков ниже скорости реально протекающих нейронных процессов. Лишь технологии ЭЭГ и МЭГ, обладающие возможностью непосредственной регистрации электрической нейронной активности, могут обеспечить получение точной временной информации о мозговых процессах неинвазивным путем. ЭЭГ и МЭГ фиксируют, соответственно, электрические и магнитные поля, порождаемые согласованной активностью популяций нейронов мозга. Среди преимуществ МЭГ по сравнению с прочими технологиями нейроимиджинга – низкая чувствительность регистрируемого магнитного поля к анизотропии электромагнитных свойств тканей и высокая плотность сенсоров, которая позволяет достичь большей точности в пространственной локализации динамики нейронных процессов (Hämäläinen et al., 1993). Кроме того, МЭГ обладает рядом существенных практических преимуществ перед другими методами функциональной нейровизуализации. Так, МЭГ-исследование проходит, как правило, в тихой обстановке, тогда как регистрация фМРТ сопровождается постоянным шумом аппаратуры. При регистрации магнитоэнцефалограммы не используются радиоактивные вещества (как в случае с ПЭТ). Перед проведением МЭГ отсутствует длительная процедура подготовки испытуемого (например, фиксации электродов, как при ЭЭГ). Все это делает МЭГ особенно удобным методом как для взрослых испытуемых, так и для маленьких детей и практически любых групп пациентов.
Метод МЭГ основан на измерении крайне слабых магнитных полей и их градиентов (с индукцией магнитного поля 10-13–10-15 тесла (Тл), что на 8–10 порядков меньше, чем у магнитного поля Земли), порождаемых электрической нейронной активностью в мозге. Регистрация магнитных полей мозга возможна благодаря использованию сверхчувствительных сенсоров магнитного поля (сквидов, или сверхпроводящих квантовых интерферометров), погруженных в жидкий гелий с температурой около 4 кельвинов.
Как следствие миниатюризации высокочувствительных сенсоров магнитного поля, в последние годы большое распространение получила технология высокоточной МЭГ (high density MEG). Высокоточные МЭГ-установки отличаются большим количеством сенсоров (до нескольких сотен), что позволяет одновременно производить запись активности многих областей мозга, получая наиболее полную картину пространственно-временных паттернов мозговой деятельности. До последнего времени эта технология была недоступной для российских исследователей, хотя в 1970–80-х годах в СССР велись разработки в области магнитоэнцефалографии. Ситуация изменилась начиная с 2010 года, когда в Московском городском психолого-педагогическом университете был установлен прибор Vectorview (компания Elekta Neuromag) для многоканальной комбинированной регистрации МЭГ и ЭЭГ. Такая установка может с точностью до долей миллисекунд записывать мозговую активность одновременно по 434 каналам (306 сенсоров МЭГ и 128 каналов ЭЭГ). Обработка регистрируемых данных требует применения математических алгоритмов пространственной фильтрации, направленных на избирательное усиление нейронных компонент измеряемого сигнала и подавление электромагнитного шума окружающего мира.
1.2. Решение обратной задачи при локализации нейронных источников методом МЭГ
При анализе данных МЭГ встает проблема решения так называемой обратной задачи (ОЗ), которая состоит в восстановлении распределения активности нейронных источников на поверхности коры головного мозга (Ilmoniemi, 1993). Решение ОЗ по определению некорректно, поскольку любая поверхностная запись может объясняться бесконечным числом различных конфигураций внутренних источников. Однако в нейрокогнитивных экспериментах можно добиться единственности решения, если ввести ограничения, основанные на когнитивных, перцептивных или иных свойствах экспериментальной задачи, а также на нашем знании функциональной анатомии мозга. Пространственная точность локализации нейронных источников обусловливается не только аппаратными характеристиками, но и методами обработки сигнала и используемыми подходами к решению обратной задачи.
Первые подходы к решению ОЗ основаны на дипольном (dipole fitting) и распределенном (minimum norm estimate) моделировании нейронных источников. К настоящему времени разработан ряд математических алгоритмов: например, методы подгонки эквивалентных токовых диполей (метод наименьших квадратов, RAP-MUSIC) (Huang et al., 2005; Mosher, Leahy, 1999), оценки, минимизирующие норму решения (MNE, MCE, LORETA) (Hämäläinen, Ilmoniemi, 1994; Pascual-Marqui et al., 1994; Uutela et al., 1999), сканирование при помощи адаптивных формирователей луча (ФЛ) – SAM, sLORETA (Pascual-Marqui, 2002; Sekihara et al., 2001; van Veen et al., 1997). Активно развиваются методы на основе различных вариантов сканирующих адаптивных ФЛ, позволяющие достичь пространственного разрешения до 0,5 см. Наиболее распространенный метод решения обратной задачи в МЭГ – minimum norm estimate, MNE (Hämäläinen et al., 1993). В его основе лежит регуляризация некорректно поставленной задачи (Тихонов, 1963) посредством введения дополнительного требования на минимальность квадратичной нормы решения (вектора токов). Этот метод основан на глобальной квадратичной минимизации и использует минимум предположений о пространственной структуре решения, выраженных в диагональности корреляционной матрицы активности нейронных источников. Метод LORETA (Pascual-Marqui et al., 1994) отыскивает максимально гладкие решения, удовлетворяющие измеренным данным. Несмотря на высокую устойчивость, оба метода обладают сравнительно низким пространственным разрешением. Метод sLORETA (Pascual-Marqui, 2002) эквивалентен одной из форм неадаптивного метода сканирующего формирователя луча и обладает несколько более высоким пространственным разрешением по сравнению с MNE и LORETA.
Среди новейших методов решения ОЗ следует выделить подходы на основе формирователей луча (ФЛ), построенные в соответствии с принципами, заимствованными из радиолокационной науки (Pascual-Marqui, 2002; Sekihara et al., 2001; van Veen et al., 1997), и позволяющие достичь пространственного суперразрешения. Фундаментальное отличие этих подходов от вышеперечисленных состоит в их локальности. Матрица обратного оператора находится построчно, т. е. отдельно для каждого узла координатной сетки в пространстве нейронных источников. Пространственное суперразрешение достигается благодаря использованию принципа адаптивности, который заключается в подавлении влияния только активных в исследуемом временном окне нецелевых источников. Отказ от глобальной оптимизации исключает необходимость использования априорной информации о пространственной корреляционной структуре активности нейронных источников.
В контексте отображения активности мозга мы заинтересованы в оценивании во времени и пространстве нейронных источников, активность которых создает определенное распределение магнитных полей, регистрируемое на поверхности головы человека. Эта проблема сводится к оценке свободных параметров модели источника – группы активных нейронов, т. е. к способам моделирования обратной задачи. Моделирование же прямой задачи в контексте МЭГ заключается в предсказании магнитных полей, которые были бы зарегистрированы сенсорами при любых значениях нейронной активности (параметра I). При моделировании прямой задачи МЭГ параметры θ рассматривают как известные и заранее заданные. В них входит геометрия головы, расположение сенсоров на поверхности головы и т. д.
Основной вход I в МЭГ – это общая электрофизиологическая активность нейронов. Экспериментальные наблюдения O – это магнитные поля, зарегистрированные на поверхности головы в условиях когнитивной или клинической парадигмы. Теоретическая модель T строится на знаниях об электродинамике (Feynman, 1963), которые сводятся в МЭГ к уравнениям Максвелла с квазистатическими предположениями (Hämäläinen et al., 1993).
Проблема реконструкции активности мозговых источников по характеру внешнего электромагнитного поля относится к широкому классу обратных задач, решаемых методами математической физики. Оценка источников магнитных полей, как и другие технологии отображения активности мозга, связана с решением обратной задачи.
Суть обратной задачи была сформулирована физиками в тех областях экспериментальной науки, где возникает нужда в сопоставлении теоретической модели с наблюдаемыми данными. Модель разрабатывается на основе теоретических знаний о природе наблюдаемого процесса, будь то климат Земли, колебания рынка акций или мозговая активность, и позволяет прогнозировать результаты реальных наблюдений.
Основной задачей математического описания является то, как от входных данных модели I получить на выходе наблюдаемые данные O путем некоторой трансформации T. Таким образом мы имеем:
O = T(I), (1) что описывает модель полученных данных O.
Входные данные I и некоторые элементы T (в том числе величины, которые могут меняться без фундаментальных нарушений в системе и, таким образом, не опровергать теоретическую модель) рассматривают как явные и неявные параметры системы в формуле (1). Разница между явной и неявной природой параметров скорее искусственная (так, в формуле (1) они не разделены) и может быть представлена следующим образом:
O = T(I, θ), (2) где θ отображает набор изначально неявных параметров в T. Предсказание наблюдений по теоретической модели с заданным набором параметров называется решением прямой задачи. Если, напротив, наблюдения используются для оценки величин некоторых параметров модели, то такая задача является обратной.
Наиболее важный из теоретических аспектов локализации нейронных источников связан с множественностью решений обратной задачи. Изменяя параметры I, мы, тем не менее, можем получать одни и те же наблюдения О на выходе системы. И наоборот, имея фиксированные данные, наблюдаемые на выходе системы, мы можем найти множество вариантов таких параметров внутри системы, которые не будут противоречить уравнению (1). Таким образом, в то время как прямая задача имеет единственное решение в классической физике, что следует из принципов причинности, обратная задача может иметь множество решений – иногда кардинально различающихся моделей.
В МЭГ, а также и в ЭЭГ ситуация критична. Как теоретически показал Гельмгольц в XIX веке, общая обратная задача, заключающаяся в нахождении источника электромагнитного поля снаружи проводника, имеет бесконечное количество решений. Таким образом, теоретически бесконечное число вариантов расположения мозговых источников будет соответствовать внешним наблюдениям электромагнитного поля в электро- и магнитоэнцефалографии. В результате решением таких задач занялись математики, специализирующиеся на проблемах плохой решаемости обратных задач. Математическим решением этих задач является добавление в модель необходимых дополнительных данных, которые можно получить из знаний в предметной области для дополнения теоретической модели. Однако и в этом случае результат решения обратной задачи может оказаться неверным. При практическом использовании результатов моделирования это может привести к драматическим последствиям. Так, например, если локализация эпилептического очага, предположительно определенная по результатам моделирования магнитных полей эпилептического спайка, не соответствует реальности, то резекции будет подвергнута здоровая мозговая ткань, а эпилептогенный очаг останется нетронутым.
Современному взгляду на математическое решение некорректных задач положили начало исследования А. Н. Тихонова в 1960-х годах и введение понятия «регуляризация», которое наглядно формализовало решение некорректных проблем (Tikhonov, 1991). Тихонов предполагал, что некоторые математические манипуляции над выражениями некорректных задач могут сделать их корректными в том смысле, что решение будет существовать и оно будет единственным. Совсем недавно для регуляризации стали использовать теорию вероятностей, в частности, байесовский подход (Tarantola, 2004) и вариационные байесовские методы, позволяющие оценить параметры априорного распределения амплитуды токовых диполей из самих данных (Attias, 2000). Таким образом, методология моделирования магнитных мозговых источников последовательно движется от методов решения обратной задачи к статистическим оценкам и выводам и приближается к другим методам функционального отображения активности мозга (Baillet et al., 2001).
2. МЭГ в картировании языка и речи
В последнее десятилетие в связи с развитием сложнейших вычислительных методов, позволяющих увеличить пространственно-временную точность локализации источников нейронной активности, выросла значимость метода МЭГ для предоперационной диагностики. Магнитоэнцефалография может служить адекватным, а иногда и наиболее информативным методом исследования вызванной и спонтанной активности коры головного мозга. В отличие от метода фМРТ, в котором активность нейронов оценивается опосредованно, т. е. по изменению локального кровотока за счет определения разницы в насыщении крови кислородом (так называемого Blood Oxygen Level Dependent, или BOLD signal), МЭГ способна обнаруживать источники, связанные с изменением суммарной постсинаптической активности нейронов. Однако чувствительность МЭГ сильно зависит от ориентации источников тока по отношению к сенсорам; максимальное поле за пределами поверхности головы генерируется источниками, ориентированными по касательной к поверхности головы. Именно такое расположение источников нейронной активности обеспечивает высокую эффективность локализации источников в области центральной борозды и височной коры. Исследование височных областей является наиболее важным при локализации речевых функций у человека (Papanicolaou et al., 2004; Valaki et al., 2004; Näätänen et al., 1997; Shestakova et al., 2002 a; Shtyrov et al., 2010 a), например, с использованием вызванных полей (магнитных аналогов вызванных потенциалов).
Благодаря оптимальной ориентации слуховой коры относительно поверхности головы и, следовательно, относительно МЭГ-сенсоров почти 100% ее активности может быть зарегистрировано при помощи сверхчувствительных датчиков в МЭГ-исследовании. Токи, генерируемые пирамидными нейронами первичной слуховой коры, направлены по касательной к поверхности головы. В результате этого линии магнитного поля выходят за пределы поверхности головы, что позволяет регистрировать сигнал наилучшим образом. Таким образом, методика МЭГ оказалась оптимальной для исследования восприятия речи – одного из наименее изученных когнитивых процессов у человека.
Долгое время речевая функция оставалась предметом исследования исключительно поведенческих и психолингвистических дисциплин, которые, к сожалению, не могли дать информации о мозговых основах речи. Позже наши знания о речи обогатились благодаря данным нейропсихологических исследований, начиная с открытий XIX века, когда впервые были описаны зоны Брока (Broca, 1861) и Вернике (Wernicke, 1874), ответственные за восприятие и генерацию речи. Работу продолжила школа А. Р. Лурии (Лурия, 1979). Было установлено, что по выпадению функции при поражении определенных зон мозга оказывается возможным локализовать ее. Лишь в конце прошлого века в связи развитием научнотехнического прогресса и появлением уникальных технологий нейроимиджинга началось активное экспериментальное изучение мозга человека, и наши знания обогатились результатами исследований функциональной нейроанатомии речи у здоровых испытуемых с использованием фМРТ и ПЭТ. Несмотря на то, что данные, полученные с помощью этих методов, представляют несомненную ценность для понимания языка, сами методы не обладают достаточным временным разрешением для исследования лингвистических процессов, так как в процессе восприятия речи в мозге происходит быстрый и динамический анализ информации на каждом уровне ее обработки. Мозг должен успевать определить звуки, классифицировать их как фонемы (т. е. именно как речевые звуки), разбить на морфемы и слова, установить между ними грамматические связи и использовать их, для того чтобы построить целостную структуру фразы и понять ее смысл. Очевидно, что для понимания механизмов речи недостаточно пользоваться исключительно данными статических оценок поведения и анатомии мозга; здесь необходимы технологии отображения мозговой активности с высоким разрешением во времени.
Как показывают исследования с использованием ЭЭГ и МЭГ, следы памяти для слов активируются при их предъявлении, что отражается в раннем (до 200 мс) всплеске активации на настоящие слова, в отличие от псевдослов, для которых отсутствует репрезентация (Shtyrov et al., 2010 a). Подобная разница (при условии, что в остальном стимулы уравнены по своим характеристикам) является признаком лексического доступа к следам памяти в «умственном словаре» (Shtyrov, 2010). В ряде исследований показано, что психофизиологические корреляты доступа к этим следам памяти отражаются в зарегистрированном сигнале МЭГ в виде активации, сконцентрированной в области верхней части левой височной доли (Näätänen et al., 1997; Shestakova et al., 2002 a, 2004; Shtyrov et al., 2005) (см. рис. 1).
Психолингвистические теории сходятся в том, что обработка речи может рассматриваться как состоящая из следующих четырех уровней: (1) уровень фонологической обработки, на котором звуки речи анализируются на предмет их фонетических/фонологических свойств; (2) лексическая обработка, которая рассматривается как поиск единиц в «умственном словаре»; (3) семантическая обработка, в ходе которой оценивается смысл единицы информации; (4) уровень синтаксиса, на котором анализируется грамматическая информация, заключенная в связи слов в общей структуре высказывания (MacKay, 1987). Растущее число исследований и в особенности МЭГ-данных, свидетельствует о скоростном и параллельном доступе к информации всех типов, как только она становится доступной: в течение временного промежутка около 100–200 мс (Shtyrov et al., 2005, 2010 а; Shtyrov, Pulvermüller, 2007 a, b; Shtyrov et al., 2010 a), а возможно, и еще раньше, от 50 мс (MacGregor, Gerstein, 1991).
Данная концепция скоростной обработки речи в мозге является пока довольно новой, однако она стремительно развивается, поскольку соответствует экологическим требованиям интерпретировать любую поступающую информацию настолько быстро, насколько это возможно. Скоростная обработка информации является критически важной для биологического выживания, поэтому нервная система развивалась с течением эволюции в направлении максимально быстрой обработки сигналов. С этой точки зрения даже 200 мс для обработки вербальной информации могут казаться не такой большой скоростью. Данные нейроанатомических и функциональных исследований говорят о том, что передача информации между улиткой внутреннего уха и корой больших полушарий по самым быстрым путям занимает не более 10–20 мс (Eldredge, Miller, 1971), дальнейшие 15–20 мс уходят на то, чтобы передать сигнал из первичных слуховых зон в нижнелобную кору (Shtyrov, Pulvermüller, 2007 b). Следовательно, существуют сильные нейробиологические доводы в пользу того, что как минимум первичное извлечение важной лингвистической информации из речи (если не интеграция ее в более широкий контекст) может быть практически немедленным, и МЭГ на данном этапе обрабоки информации незаменима для картирования речевой функции. Методика записи МЭГ и совместной записи ЭЭГ и МЭГ уже привела к ряду открытий в области изучения нейробиологических основ речи. Кроме того, она является клинически перспективной с точки зрения исследования нарушений мозговых механизмов речевой функции и предоперационного картирования речевых зон. Таким примером приложений МЭГ является оценка латерализации речевой функции как при предоперационной диагностике (Mäkelä et al, 2006, 2007), так и в связи с диагностикой различных заболеваний, связанных с нарушениями речи и прочих когнитивных функций. Например, у детей с диагнозом краниостеноз была обнаружена аномальная латерализация (вплоть до полного отсутствия активации в правом полушарии) ответа M200 на разнообразные типы слуховых стимулов – от гармонических тонов и щелчков до пения птиц (Hukkie et al., 2003).

Рис. 1. Пример магнитных ответов мозга типичных испытуемых на речевые стимулы: (a) Типичный пример ответов, зарегистрированных на одном градиометре (типе сенсоров) над слуховой корой каждого полушария. Магнитный компонент негативности рассогласования (мНР) представлен разностью (жирная линия) между ответами на стандартные стимулы (пунктирная линия) и на девиантные стимулы (тонкая линия); (b) Карты топографии силовых линий магнитного поля (шаг 8 фТл) для мНР над каждым полушарием, наложенные на сенсоры, образующие форму МЭГ-шлема. Стрелки указывают расположение и ориентацию токовых дипольных источников мНР. Пунктиром отмечены магнитные линии, идущие внутрь головы, сплошными кривыми – магнитные линии, идущие из головы; (c) Слева: местоположение токовых диполей – источников мНР в каждом полушарии типичного испытуемого, наложенных на индивидуальную МРТ. Диполи спроецированы на плоскость, ближайшую к двум источникам на уровне латеральной борозды. Справа: соответствующее усредненное местоположение, отмеченное кругами (пять праворуких испытуемых), для диполей мНР в вертикальной и горизонтальной плоскостях. Стандартная ошибка расположения усредненных диполей мНР варьировала от 1 до 3 мм. Диаметр двух кругов пропорционален соответствующим средним значениям силы правого и левого диполей; (d) Результаты анализа межполушарной асимметрии по данным МЭГ-картирования: относительная и абсолютная (в скобках) сила диполей мНР для восьми праворуких и одного леворукого испытуемого в правом и левом полушариях (адаптировано из: Shestakova et al., 2002 a)
3. Магнитоэнцефалография в психофизиологии развития
Как уже отмечалось выше, относительно высокое пространственное разрешение МЭГ по сравнению с ЭЭГ связано с тем фактом, что метод МЭГ не чувствителен к неравномерностям проводимости кожи, черепа и мозговых оболочек: магнитное поле без помех проникает сквозь ткани организма. В результате МЭГ позволяет локализовать источник активации в пространстве с большей степенью точности. Кроме того, МЭГ является бесконтактным методом локализации активности мозга и не требует использования ни электродов, ни электропроводной пасты для их наложения на поверхность головы испытуемого. Такие достоинства магнитоэнцефалографии делают этот метод уникальным инструментом для исследования мозга человека и особенно детей раннего возраста (рис. 2).
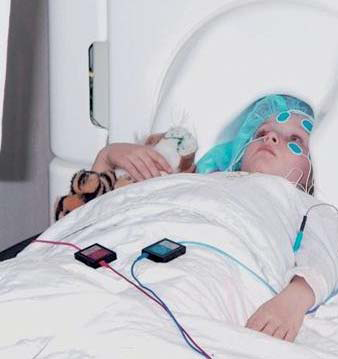
В исследованиях слуховой функции у детей наряду с наиболее широко используемым компонентом N1 вызванных потенциалов (ВП), возникающим в ответ на предъявление каждого стимула (так называемый onset response) (Näätänen et al., 1987), все большую популярность приобретает компонент, известный как негативность рассогласования (НР) (mismatch negativity, MMN). НР и магнитная НР (мНР) являются коррелятами сенсорной памяти (Näätänen, Winkler, 1999), так как возникают в ответ на рассогласование редкого (девиантного) стимула с моментальным следом памяти, сформированным часто повторяющимся (стандартным) стимулом. В более поздних исследованиях с использованием речевых стимулов выяснилось, что мНР является также коррелятом долговременной памяти, локализованной у взрослых в левом полушарии (Näätänen et al., 1997). У взрослых мНР обусловлена кортикокортикальными взаимодействиями, в то время как у детей аналогичные ответы могут быть активированы таламокортикальными проекциями (Huotilainen et al., 2008). Если у взрослых людей N1 является самым распространенным компонентом ВП, то у детей эта реакция быстро затухает (Karhu et al., 1997) и при суммации ответов наиболее видимым экзогенным ответом становится N200 (M200) – основной компонент слуховых ВП у детей (Ceponiene et al., 2002; Kushnerenko et al., 2002; Shestakova et al., 2003). Его пик, в отличие от пика N1 взрослых, приходится на 200 мс после начала предъявления стимула. Структура же мНР у детей сходна с ответом взрослых (Huotilainen et al., 2003; Sambeth et al., 2006). Так, в исследовании мНР было показано, что младенец еще до своего рождения способен различать разницу между звуками по частоте почти в такой же степени, как и взрослые (Huotilainen et al., 2003). В более позднем исследовании удалось зарегистрировать мНР у новорожденных детей в ответ на предъявление комплексных звуковых сигналов, представляющих собой суперпозицию нескольких гармоник (Sambeth et al., 2006). Аналогичные данные были получены в экспериментах других авторов (Kujala et al., 2004; Pihko et al., 2004).
На рис. 3 приводится типичный пример компонента M200, зарегистрированного в ответ на предъявление фонем родного языка детям младшего школьного возрата. Компонент локализуется в области слуховой коры, это иллюстрируется распределением амплитуд вызванных магнитных полей; мНР регистрируется в виде разницы между ответами на стандартный и девиантный стимулы (подробности экспериментальной задачи см.: Huotilainen et al., 2008; Shestakova et al., 2002 a). Локализация источника активности M200 (рис. 3) проводилась методом эквивалентных диполей, по одному диполю на каждое полушарие. Ориентация диполя совпадает с исходными представлениями о том, что на МЭГ и ЭЭГ мы наблюдаем активацию пирамидных нейронов, расположенных перпендикулярно поверхности слуховой коры. При локализации источников использован метод структурной МРТ мозга испытуемого. Источники активности, связанной с обработкой речевого сигнала, локализуются в извилине Гешля.
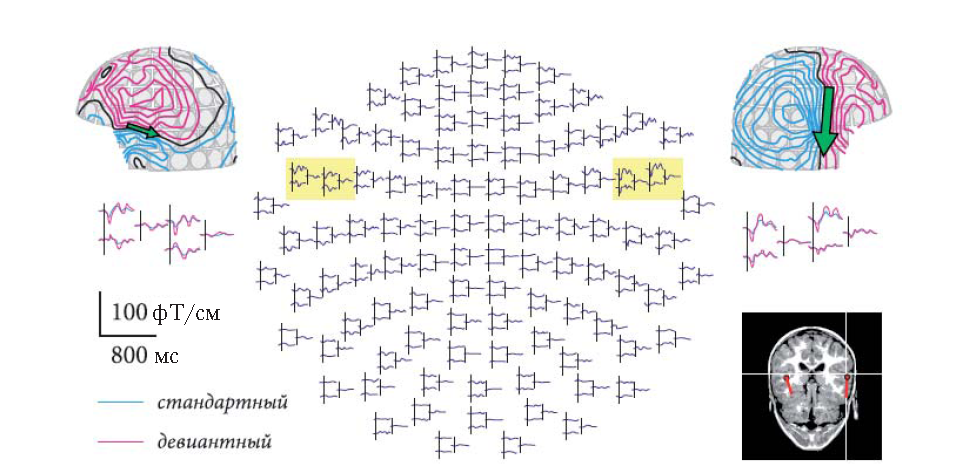
Рис 3. Пример магнитного компонента негативности рассогласования (мНР) у 7-летнего испытуемого в ответ на предъявление гласных фонем родного языка. Активность мНР выражена в виде разницы между стандартным и девиантным ответами на кривых вызванных магнитных полей, а также в виде стрелок, символизирующих токовые диполи. Пик основного компонента вызванных полей (ВПол) M200 у детей младшего школьного возраста приходится на 200 мс после начала предъявления стимула. Компонент отчетливо наблюдается в области слуховой коры в виде кривых вызванных магнитных полей
На рис. 4 показана та же активация M200, что и на рис. 3, но в виде «облака» в пространстве, а не точки: здесь использовалась модель распределенной активности без ограничения количества диполей в отдельном полушарии – метод наименьшей нормы токов, в частности – метод визуализации результатов локализации минимальной L1-нормы, известный также как метод minimum current estimate, или МСЕ. В данном случае алгоритм минимизирует сумму абсолютных значений амплитуд токов (Uutela et al., 2001). Стрелками на моделях мозга обозначены источники с максимальной амплитудой в области интереса – височных долях мозга, где находится слуховая кора. Метод L2-нормы (также известный как Euclidian l2 norm), используется не менее широко и реализован, к примеру, в некоммерческом программном обеспечении MNE (MNE-Suite, разработанном Матти Хямяляйненом (Martinos Center, Гарвард, США)), а также SPM (Functional Imaging Laboratory, UCL, Лондон, Великобритания). В этом случае, когда неизвестных переменных (амплитуд диполей) больше, чем измеренных данных, среди множества всех пространственных распределений амплитуд диполей, удовлетворяющих измеренным данным, выбирают такое распределение, чтобы сумма квадратов амплитуд диполей была наименьшей – решение с минимальной энергией.
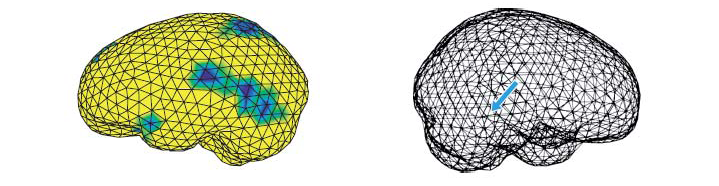
Рис. 4. Визуализация той же активности M200, что и на рис. 2, но в виде облака в пространстве, а не точечного диполя: здесь используется модель распределенной активности без ограничения количества диполей в отдельном полушарии (в частности, метод L1-нормы, или МСЕ). Стрелкой обозначены источники с максимальной амплитудой в области интереса – в височных областях мозга, где находится слуховая кора
Несмотря на существующие методологические сложности, связанные в основном с большей удаленностью коры головного мозга младенцев и маленьких детей от МЭГсенсоров (Pang et al., 2003) и неконтролируемой подвижностью юных испытуемых, источники активности могут быть достаточно точно локализованы в слуховой коре (рис.4). Это стало возможным при использовании системы постоянного отслеживания положения головы по отношению к сенсорам магнитоэнцефалографа. Кроме того, интеграция со структурной МРТ позволяет учитывать индивидуальную анатомию мозга.
Магнитоэнцефалография может служить оптимальным методом исследования вызванной и спонтанной активности не только слуховой коры, но и других областей мозга, например, соматосенсорной коры. Так, метод МЭГ успешно применяли для тестирования дифференцированного влияния стадии сна, в котором находились новорожденные, на их чувствительность к тактильной стимуляции (Pihko et al., 2004; Pihko, Lauronen, 2004). В данной работе впервые были зарегистрированы соматосенсорные ответы у новорожденных при помощи МЭГ (рис. 5). Исследование также показало, что на стадии активного или поверхностного сна амплитуда соматосенсорных вызванных полей была меньше, чем в состоянии глубокого сна. Следует упомянуть о клинических приложениях метода МЭГ, основными из которых в педиатрии являются локализация источников судорожной активности в неокортексе, а также дифференциация фокальной и генерализованной форм эпилепсии как метод предоперационной диагностики (Mäkelä et al., 2006, 2007). Эта методика успешно применяется для обследования как взрослых пациентов, так и детей.
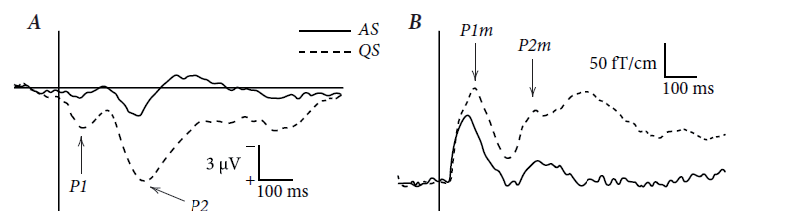
Рис. 5. Пример электрических (А) и магнитных (B) соматосенсорных вызванных ответов, зарегистрированных у новорожденных при тактильной стимуляции. Пунктирная линия – спокойный сон, сплошная – активированный сон. Вертикальными линиями отмечено начало тактильной стимуляции (Pihko et al., 2004. С разрешения Elsevier)
4. Использование МЭГ в предоперационной диагностике и определении источников интериктальных спайков
С появлением метода регистрации соматосенсорных вызванных полей появилась возможность картировать активность в моторных и соматосенсорных областях с высоким пространственным и временным разрешением (Mäkelä et al., 2006 ; Salenius et al., 1997; Sutherling et al., 1988). Необходимо заметить, что о сохранности данных областей в первую очередь заботятся во время нейрохирургического вмешательства.
Наряду с принципом локализации латерализация является одним из базовых принципов организации функциональной активности мозга. К примеру, развитие уникальной способности человека говорить, т. е. формулировать и формировать речевые сообщения, а также воспринимать и понимать речь других людей, привело в эволюции к латерализации речевой функции в мозге человека, а именно доминированию левого полушария у подавляющего большинства людей.
У 90 % праворуких людей доминирующим по речи является левое полушарие, но в остальных случаях имеет место «атипичное» распределение речевой функции по полушариям (Benson, 1978). Это диктует необходимость определения латерализации речевой функции во всех случаях оперативного вмешательства, когда могут быть затронуты речевые области левого полушария либо их гомологи в правом полушарии головного мозга. Первичные сенсорные, моторные зоны и речевые центры относятся к невосполнимым зонам мозга. Когда существует опасность нарушить эти зоны вследствие оперативного лечения неврологических заболеваний (опухоли мозга, резистентные формы эпилепсии), требуется тщательное планирование нейрохирургического вмешательства. До сих пор одним из основных методов предоперационной диагностики латерализации функций мозга является интракаротидный амобарбиталовый тест, который проводится, чтобы выяснить, какое полушарие мозга пациента контролирует память, а также его способность говорить и понимать речь. Эта информация необходима хирургу для предотвращения таких осложнений, как нарушения речи при операциях на височной доле. Интракаротидный амобарбиталовый тест был введен в клиническую практику канадским нейропсихологом Вадой (Juhn A. Wada) и носит его имя. Во время тестирования, проводимого специалистомангиографом, пациенту вводится через катетер во внутреннюю сонную артерию снотворное вещество амобарбитал. При введении амобарбитала в правую сонную артерию правое полушарие мозга «засыпает», т. е. перестает функционировать на несколько минут, тогда как левое полушарие продолжает работать. При введении в левую сонную артерию все происходит наоборот: левое полушарие «засыпает», а правое продолжает нормально работать. После введения амобарбитала врач-нейропсихолог проводит различные тесты, проверяя речь и память пациента. Если, например, при «отключении» левого полушария у испытуемого пропадает речь, а при «отключении» правого полушария она остается ненарушенной, то делается вывод о том, что способность пациента говорить контролируется левым полушарием.
Инъекции препарата нередко сопровождаются нарушением сознания пациентов в виде спутанности, сонливости или психомоторного возбуждения независимо от вида анестетика, что, по-видимому, связано с кумулятивным эффектом препарата. Избежать такого эффекта возможно, если проводить исследования в разные дни, но это повышает риск осложнений. Вот почему весьма перспективным представляется использование современных неинвазивных методов картирования функций мозга, в первую очередь методики МЭГ, которая чувствительна к быстрым динамическим изменениям в активности, генерируемой в речевых областях. Особый интерес представляет в этой связи парадигма, разработанная исследователями Университета Хьюстона, США (Simos et al., 1998). Использовалась задача на определение совпадения или несовпадения значений слов в пределах определенных категорий: например, апельсин и яблоко совпадают, потому что являются фруктами, а груша и молоток – нет, так как относятся к разным смысловым категориям. Еще в 1988 году с использованием этой парадигмы было показано, что в 87 % случаев магнитные ответы мозга локализовались в левом полушарии, что совпадало с процентом левополушарного доминирования, известного по данным предыдущих исследований, включая инвазивный тест Вады (Simos et al., 1998). Эти закономерности подтвердились в целой серии МЭГисследований испытуемых, говорящих на разных языках (Breier et al., 1999), с использованием парадигмы на распознавание слов. Оказалось, что в ответ на предъявление слова первичные области слуховой коры активируются билатерально, тогда как активность вторичных и ассоциативных областей четко латерализована в левом полушарии. Особый интерес вызывают исследования Центра когнитивных исследований в Хельсинки (Финляндия), где, используя такие простые стимулы, как фонемы, было установлено, что, тогда как у 10 из 10 праворуких испытуемых ответы были латерализованы в левом полушарии, у случайно попавшего в выборку леворукого испытуемого источник нейронной активности локализовался в правом полушарии (Shestakova et al., 2002 a). Таким образом, эти и другие исследования латерализации речи методом МЭГ дают основание предполагать, что неинвазивное МЭГ-обследование может быть использовано для определения латерализации на индивидуальном уровне и позволит заменить инвазивный амобарбиталовый тест.
МЭГ также позволяет локализовать источники судорожной активности в неокортексе и дифференцировать фокальную и генерализованную эпилепсию (Mäkelä et al., 2006, 2007). Эпилептическая активность намного четче выражена на магнитоэнцефалограмме по сравнению с электроэнцефалограммой. Кроме того, при помощи МЭГ возможно визуализировать вектор распространения патологической активности во времени и пространстве как внутри полушария, так и между полушариями мозга, используя, например, метод локализации множественных диполей (Hari et al., 1993; Lin et al., 2003; Paetau et al., 1999).
Недавние разработки в области обнаружения межприступной пароксизмальной активности привели к появлению автоматических методов анализа и обнаружения очагов на поверхности коры (Ossadtchi et al., 2004). Использование парадигмы скрытых марковских цепей позволило разработать методику оценивания каузальной структуры мультифокальной межприступной активности (Ossadtchi et al., 2005). Такой анализ в дальнейшем может помочь в выявлении зон инициации приступов среди множества зон ирритации и спланировать с учетом этих данных хирургическое вмешательство.
Заключение и выводы
МЭГ является инновационным, высокотехнологичным нейрофизиологическим методом. Слабые магнитные поля (порядка 10-15 Тл), генерируемые нейронами головного мозга, бесконтактно улавливаются сверхчувствительными датчиками (сквидами). МЭГ обладает рядом преимуществ перед ЭЭГ, среди которых – точная пространственная локализация источника активности в коре головного мозга. Кроме того, МЭГ обладает высоким (миллисекундным) временным разрешением, что чрезвычайно важно для локализации динамических когнитивных процессов во времени, в частности, речевой функции. В клинике этот метод зарекомендовал себя как эффективный способ локализации эпилептической активности. В некоторых случаях пространственная точность картирования соматосенсорных областей мозга методом МЭГ превосходит возможности фМРТ. Дальнейшее развитие метода, как нам представляется, будет направлено, с одной стороны, на усовершенствование технологии записи электромагнитной активности мозга и на разработку новых математических алгоритмов обработки сигнала с целью повышения чувствительности метода и точности пространственно-временной локализации нейронной активности в мозге. С другой стороны, в ближайшие годы развитие клинических аспектов МЭГ, вероятно, будет вестись в первую очередь в области предоперационного картирования мозговых функций, а также в определении источников патологической активности в мозге и в диагностических исследованиях неврологических и психиатрических расстройств.
Литература
- Лурия А. Р. Язык и сознание / Под ред. Е. Д. Хомской. М.: Изд. МГУ, 1979.
- Тихонов А. Н. О регуляризации некорректно поставленных задач // Докл. АН СССР. 1963. Т. 153. C. 49–53.
- Attias H. A variational Bayesian framework for graphical models // Advances in Neural Information Processing Systems / Eds. S. A. Solla, T. K. Leen, K. Müller. Cambridge, MA. 2000. V. 12. P. 209–215.
- Baillet S., Mosher J. C., Leahy R. M. Electromagnetic brain mapping // IEEE Signal Processing Magazine. 2001. V. 18. P. 14–30.
- Benson D. F. Neurological correlates of aphasia and apraxia // Recent advances in clinical neurology / Eds. W. B. Matthews, G. Glaser. London, 1978. P. 163–175.
- Breier J. I. et al. Lateralization of cerebral activation in auditory verbal and non-verbal memory tasks using magnetoencephalography // Brain Topography. 1999. V. 12. P. 89–97.
- Broca P. Remarques sur la siège de la faculté de la parole articulée, suivies d'une observation d'aphémie (perte de parole) // Bulletin de la Société d'Anatomie. 1861. V. 36. P. 330–357.
- Ceponiene R. et al. Event-related potential features indexing central auditory discrimination by newborns // Brain Res. Cogn. Brain Res. 2002. V. 13. P. 101–113.
- Eldredge D. H., Miller J. D. Physiology of hearing // Annu Rev Physiol. 1971. V. 33. P. 281–310.
- Feynman R. P. The Feynman Lectures on Physics. Reading, Mass. V. 2. 1963.
- Hämäläinen M. S. et al. Magnetoencephalography – theory, instrumentation, and applications to noninvasive studies of the working human brain // Rev. Mod. Phys. 1993. V. 65. P. 413–497.
- Hämäläinen M. S., Ilmoniemi R. J. Interpreting magnetic fields of the brain: minimum norm estimates // Med Biol Eng Comput. 1994. V. 32. P. 35–42.
- Hari R. et al. Parietal epileptic mirror focus detected with a whole-head neuromagnetometer // Neuroreport. 1993. V. 5. P. 45–48.
- Huang M. et al. Vector-based spatial-temporal minimum L1-norm solution for MEG // NeuroImage. 2005. V. 31. P. 1025–1037.
- Hukkie J. et al. Measurements of electrical and magnetic brain activity help detecting brain dysfunctions in children with craniosynostoses // Proceedings of the Tenth International Congress of the International Society of Craniofacial Surgery. Monterey, USA. 2003.
- Huotilainen M. et al. Auditory magnetic responses of healthy newborns // Neuroreport. 2003. V. 14. P. 1871–1875.
- Huotilainen M., Shestakova A., Hukki J. Using magnetoencephalography in assessing auditory skills in infants and children // Int. J. Psychophysiol. 2008. V. 68. P. 123–129.
- Ilmoniemi R. J. Models of source currents in the brain // Brain Topography. 1993. V. 5. P. 331–336.
- Karhu J. et al. Dual cerebral processing of elementary auditory input in children // Neuroreport. 1997. V. 8. P. 1327–1330.
- Kujala T. et al. Long-term exposure to noise impairs cortical sound processing and attention control // Psychophysiology. 2004. V. 41. P. 875–881.
- Kushnerenko E. et al. Maturation of the auditory change detection response in infants: a longitudinal ERP study // Neuroreport. 2002. V. 13. P. 1843–1848.
- Lin Y. Y. et al. Magnetoencephalographic analysis of bilaterally synchronous discharges in benign rolandic epilepsy of childhood // Seizure. 2003. V. 12. P. 448–455.
- MacGregor R. J., Gerstein G. L. Cross-talk theory of memory capacity in neural networks // Biol. Cybern. 1991. V. 65. P. 351–355.
- MacKay D. G. The organization of perception and action // A theory of language and other cognitive skills. NY, 1987.
- Mäkelä J. P. et al. Magnetoencephalography in neurosurgery // Neurosurgery. 2006. V. 59. P. 493–510.
- Mäkelä J. P. et al. Magnetoencephalography in neurosurgery // Neurosurgery. 2007. V. 61. P. 147–164.
- Mosher J. C., Leahy R. M. Source Localization Using Recursively Applied And Projected (RAP) MUSIC // IEEE Signal Proces. 1999. V. 47. P. 332–340.
- Näätänen R. et al. The mismatch negativity to intensity changes in an auditory stimulus sequence // Electroencephalography and Clinical Neurophysiology. 1987. V. 40. P. 125–131.
- Näätänen R. et al. Language-specific phoneme representations revealed by electric and magnetic brain responses // Nature. 1997. V. 385. P. 432–434.
- Näätänen R., Winkler I. The concept of auditory stimulus representation in cognitive neuroscience // Psychological Bulletin. 1999. V. 12. P. 826–859.
- Ossadtchi A. et al. Automated interictal spike detection and source localization in magnetoencephalography using independent components analysis and spatiotemporal clustering // Clin. Neurophysiol. 2004. V. 115. P. 508–522.
- Ossadtchi A. et al. Hidden Markov modeling of spike propagation from interictal MEG data // Phys. Med. Biol. 2005. V. 50. P. 3447–3469.
- Paetau R. et al. Magnetoencephalography in presurgical evaluation of children with the Landau-Kleffner syndrome // Epilepsia. 1999. V. 40. P. 326–335.
- Pang E. W. et al. Localization of auditory N1 in children using MEG: source modeling issues // International Journ. of Psychophysiology. 2003. V. 51. P. 27–35.
- Papanicolaou A. C. et al. Magnetocephalography: a noninvasive alternative to the Wada procedure // Journ. of Neurosurgery. 2004. V. 100. P. 867–876.
- Pascual-Marqui R. D., Michel C. M., Lehmann D. Low resolution electromagnetic tomography: a new method for localizing electrical activity in the brain // International Journ. of Psychophysiology. 1994. V. 18. P. 49–65.
- Pascual-Marqui R. D. Standardized low-resolution brain electromagnetic tomography (sLORETA): technical details // Methods Find. Exp. Clin. Pharmacol. 2002. V. 24. P. 5–12.
- Pihko E. et al. Auditory evoked magnetic fields to speech stimuli in newborns-effect of sleep stages // Neurol. Clin. Neurophysiol. 2004. V. 2004. P. 6.
- Pihko E., Lauronen L. Somatosensory processing in healthy newborns // Exp. Neurol. 2004. V. 190. P. S2–7.
- Salenius S. et al. Cortical control of human motoneuron firing during isometric contractions // J. Neurophysiol. 1997. V. 77. P. 3401–3405.
- Sambeth A. et al. Newborns discriminate novel from harmonic sounds: a study using magnetoencephalography // Clinical Neurophysiology. 2006. V. 117. P. 496–503.
- Sekihara K. et al. Reconstructing spatio-temporal activities of neural sources using an MEG vector beamformer technique // IEEE Trans. Biomed. Eng. 2001. V. 48. P. 760–771.
- Shestakova A. et al. Involuntary attention in children as a function of sound source location: evidence from event-related potentials // Clin. Neurophysiol. 2002 a. V. 113. P. 162–168.
- Shestakova A. et al. Abstract phoneme representations in the left temporal cortex: magnetic mismatch negativity study // Neuroreport. 2002 b. V. 13. P. 1813–1816.
- Shestakova A. et al. Event-related potentials associated with second language learning in children // Clin. Neurophysiol. 2003. V. 114. P. 1507–1512.
- Shestakova A. et al. Orderly cortical representation of vowel categories presented by multiple exemplars // Brain Res. Cogn. Brain Res. 2004. V. 21. P. 342–350.
- Shtyrov Y., Pihko E., Pulvermüller F. Determinants of dominance: is language laterality explained by physical or linguistic features of speech? // Neuroimage. 2005. V. 27. P. 37–47.
- Shtyrov Y., Pulvermüller F. Language in the mismatch negativity design: motivations, benefits and pro-spects // Journ. of Psychophysiology. 2007 a. V. 21. P. 176–187.
- Shtyrov Y., Pulvermüller F. Early MEG activation dynamics in the left temporal and inferior frontal cortex reflect semantic context integration // Journ. Cogn. Neurosci. 2007 b. V. 19. P. 1633–1642.
- Shtyrov Y. Automaticity and attentional control in spoken language processing: neurophysiological evidence // Mental Lexicon. 2010. V. 5. P. 255–276.
- Shtyrov Y., Kujala T., Pulvermüller F. Interactions between language and attention systems: early automatic lexical processing? // J. Cogn. Neurosci. 2010 a. V. 22. P. 1465–1478.
- Shtyrov Y., Nikulin V. V., Pulvermüller F. Rapid cortical plasticity underlying novel word learning // Journ of Neuroscience. 2010 b. V. 30. P. 16864–16867.
- Simos P. G. et al. Assessment of functional cerebral laterality for language using magnetoencephalography // Journ. of Clinical Neurophysiology. 1998. V. 15. P. 364–372.
- Sutherling W. W. et al. The magnetic and electric fields agree with intracranial localizations of somatosensory cortex // Neurology. 1988. V. 38. P. 1705–1714.
- Tarantola A. Inverse Problem Theory and Methods for Model Parameter Estimation. Philadelphia, 2004.
- Tikhonov A. N. lll-Posed Problems in Natural Sciences. Utrecht, Tokyo, Moscow, 1991.
- Uutela K., Hämäläinen M., Somersalo E. Visualization of magnetoencephalographic data using minimum current estimates // NeuroImage. 1999. V. 10. P. 173–180.
- Uutela K., Taulu S., Hämäläinen M. Detecting and correcting for head movements in neuromagnetic measurements // NeuroImage. 2001. V. 14. P. 1424–1431.
- Valaki C.E. et al. Cortical organization for receptive language functions in Chinese, English, and Spanish: a cross-linguistic MEG study // Neuropsychologia. 2004. V. 42. P. 967–979.
- van Veen B.D. et al. Localization of brain electrical activity via linearly constrained minimum variance spatial filtering // IEEE Trans. Biomed. Eng. 1997. V. 44. P. 867–880.
- Wernicke C. Der aphasische Symptomencomplex. Eine psychologische Studie auf anatomischer Basis. Breslau, 1874.
Информация об авторах
Метрики
Просмотров web
За все время: 20032
В прошлом месяце: 145
В текущем месяце: 64
Скачиваний PDF
За все время: 2764
В прошлом месяце: 40
В текущем месяце: 24
Всего
За все время: 22796
В прошлом месяце: 185
В текущем месяце: 88